
자체 개발 항암제 신약 뮤신1에 대하여
여러 암 종 타겟 가능하고, 전임상에서 우수한 효능
뮤신1(Muc1)은 세포표면 당단백질로 다양한 암과 암 줄기세포에서 높게 발현되는 특성을 갖고 있다.
뮤신1의 과발현은 유방암, 결장암, 난소암, 폐암 및 췌장암 등과 관련 있는 것으로 알려져 있다.
당화(glycosylation)가 성장인자에 결합하는데, 많은 양의 뮤신1을 생산하는 암 세포가 수용체 근처에 성장 인자를 집중시켜 수용체 활성을 증가시키고 암세포의 성장을 가능하게 한다.
PAb001은 암 세포에 과다 발현되는 MUC1을 타겟하는 정밀 표적 항암 항체신약이다.

삼중음성유방암(TNBC, Triple Negative Breast Cancer)은 전체 유방암의 15~20%를 차지하며, 무진행 생존기간이 평균 6개월 미만으로 치료가 어려운 암이다.
삼중음성 유방암 치료는 항암화학요법을 수술 전에 시행하는데, 선행 항암치료 받은 약 60~80%의 환자에서 암이 완전히 소멸되지 않아 재발율이 높고 예후도 좋지 않다.
’19.3월 티쎈트릭이 면역항암제 중 첫번째로 화학치료제 아브락산과 병용 TNBC 1차 치료 사용 승인을 받았다.
티쎈트릭의 무진행생존기간(PFS) 중앙값은 7.2개월, 위약은 5.5개월이다.
로슈의 유방암치료제 캐싸일라도 전이성 유방암 적응증으로 사용되고 있다.
GlobalData는 로슈의 케싸일라의 순현재가치(NPV)를 $2.5bn(약 3조원)으로 평가하고 있다.
동사는 삼중음성유방암 전임상 모델에서 로슈의 캐싸일라 대비 종양크기에 의미 있는 결과를 확인하였다.

뮤신1이 발현되는 암은 약 12종으로 타겟 시장이 크다는 장점을 갖고 있다.
최근 항암제 거래 트랜드를 살펴보면 데이터가 긍정적이면서 여러 암 종을 타겟하는 경우 기술 수출이 비교적 용이하고 큰 규모로 이루어지고 있다.
동사는 ’19.5월 글로벌 제약사와 PAb001에 대해 물질이전계약(MTA)를 체결해 기술수출을 위한 기술 검증단계에 있다.

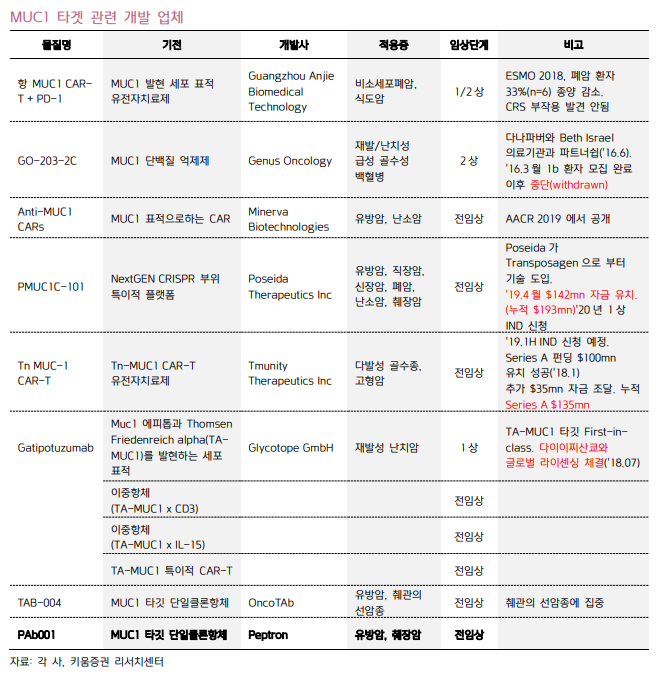
뮤신1 타겟 잠재 경쟁 업체
연구개발 단계 대부분 초기이며, 타겟력을 높이려는 시도
같은 타겟을 공략한다는 것은 잠재 경쟁 업체가 될 가능성도 있지만, 타겟 물질에 대해 성공 가능성과 시장성을 높이 평가한다는 의미도 된다는 점에서 꼭 나쁘다고 볼 수 없다.
MUC1 타겟으로 CAR-T, 항체 등 여러 형태로 개발되고 있으며, 개발 단계는 아직 전임상~1/2상 단계에 있다.
MUC1 타겟이 암세포에 특이적 부위에 결합을 하게 하기 위해 CAR-T, CAR와 같은 키메릭 항원 수용체를 이용하려는 시도로 보인다.
동사는 암세포 특이적 부위에 결합하는 경쟁력을 갖고 있는 것으로 보인다.
비상장 바이오텍 업체들이 MUC1 관련 개발을 하고 있는데, 초기 자금 유치에서 규모가 꽤 높은 것이 특징이었으며, 다이이찌산쿄는 Glycotope와 라이센싱을 체결해 MUC1에 관심을 갖고 있는 것으로 보인다.
GLP-1 파킨슨 치료제
임상 성공 가능성 높아
파킨슨병은 도파민 부족으로 일어나는 현상이기 때문에 주된 치료 요법으로 도파민을 보충해주는 것을 사용한다.
도파민이 뇌혈관장벽(BBB)를 통과하지 못하기 때문에 L-dopa를 사용해 BBB 통과해 뇌에 도달해 뉴런이 도파민으로 전환시킨다.
다만, 레보도파는 사용 이후 6년 이상 경과시 약 75%의 환자들은 이상운동증 등의 다른 합병증이 생기기 때문에 환자의 연령 등을 고려해야한다.
도파민효능제는 레보도파 대비 이상운동증을 덜 유발하지만, 고령 환자의 경우 혼동이나 환각을 잘 일으킬 수 있다는 부작용이 있다.
이렇듯 파킨슨병은 미충족 의료 수요가 높은 질병이다.
동사는 미국 국립보건원(NIH)로부터 GLP-1제제 퇴행성 뇌질환 용도특허 전용실시권을 ‘14년 확보하여 현재 국내 2상 중이다.
GLP-1 제제는 여러 논문을 통해 파킨슨병에 치료 효과를 나타낸 바 있다.
University College London 연구팀이 Bydureon으로 62명 중등도 파킨슨 환자 대상으로 1년간 투약한 결과 운동 증상 개선을 보였으며, 복용 중단한 후 12주가 지난 후에도 지속되었다.
Cedars-Sinai Medical Center에서도 노보노 디스크의 GLP-1 제제 빅토자를 가지고 57명 대상 파킨슨 2상 연구 중에 있다.
과거 연구들에 의하면 인슐린 신호 전달 경로 장애로 파킨슨병이 생길 수 있어 당뇨병과 신경 퇴행성 질환과 연관성을 제시한 바 있다.
GLP-1 수용체는 중추 신경계에 존재하며 자극을 받으면 세포 생존과 신경 보호를 촉진할 수 있는 역할을 한다.
다만, 짧은 반감기와 BBB 통과 등이 치료의 제약으로 남아있는데, 동사의 PT302는 장기 방출제제다.
파킨슨병 Rat 모델에서 PT302 단회 투여로 20일 넘게 쥐의 혈장에서 높은 수준의 exendin-4가 유지되었다.
PT302 치료 후 뇌 손상이 있는 쥐의 뇌에 도파민 활성화 뉴런을 측정하는 티로신 수산화 효소 면역반응(TH-IR)이 현저히 증가하였다.
영국 런던대 Dr. Foltynie 교수가 파킨슨 환자 68명 대상으로 GLP-1 약물의 파킨슨병 치료 효과에 대해 연구한 결과 투약 48주까지 대조군(레보도파) 대비 -4.3포인트의 격차를 나타냈다.
PT302는 지속형제제로 뇌벽을 더 잘 통과하여 뇌 안에 지속적으로 약효가 남아있을 것으로 추측되기 때문에 2상에서 긍정적인 효능을 나타내어 성공 가능성이 높을 것으로 기대하고 있다.

울산대 의과대학 서울중앙병원 신경과학교실의 ‘파킨슨병 치료’에 관한 자료에 의하면, 파킨슨병치료의 일반 원칙은 신경보호작용이 있는 약이 있다면 우선적으로 투여하는 것으로 2상에서 PT302의 신경보호작용 또한 확인된다면 향후 상용화 성공 가능성도 높다 할 수 있겠다.
GLP-1제제의 퇴행성 뇌질환 전세계 독점권의 1차 특허는 ‘25년 만료이며, 최근 치료용도의 특허를 추가로 확보했다.
또한, 미국은 신규 적응증에 대해 3년 독점기간을 부여하고, 특허 존속기간이 얼마남지 않은 의약품 대상으로 5년간 특허기간 연장해주는 제도도 운영하고 있다.
PT302는 ‘19년 하반기 첫 환자 투약을 시작으로 약 1년간의 임상을 걸쳐 ‘20년 하반기 국내 2상 완료 후 기술수출을 목표로 하고 있다.
파킨슨병치료제 외에 레보도파 유발 이상운동증(LID, Levodopa Induces Dyskinesia) 적응증과 외상성 뇌손상(TBI) 적응증으로도 확장하여 전임상 개발 중에 있다.
코넥스에 상장된 카이노스메드는 FAF1(Fas-Associated Factor1)로 국내 파킨슨치료제 1상 완료하고 미국 2상 준비 중에 있으며, 카이노스메드 시가총액은 약 2,400억원이다.
디앤디파마텍은 최근 시리즈 B 단계에서 1,400억원의 투자 유치를 마무리 했으며, 3,800억원의 투자 후 기업가치 평가를 받았다.
디앤디파마텍의 자회사 뉴랄리가 신경 퇴행성 질환 치료제를 개발 중이다.
GlobalData에 따르면 주요 파킨슨 치료제가 증상 완화제 임에도 불구하고 평균 순현재가치(NPV) 약 6,000억원대를 형성하고 있다.

리포트 원문 link : http://hkconsensus.hankyung.com/apps.analysis/analysis.downpdf?report_idx=526193
Investory 인베스토리 텔레그램 메신저 채널에 입장해서 새로운 글 알림 받기 : https://t.me/investory123



